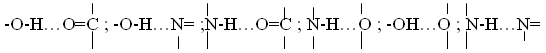Как пример водородных связей можно привести взаимодействие молекул воды. Т.к. атом кислорода в молекуле воды имеет еще две неподеленные электронные пары, он несет частично отрицательный заряд. Как более отрицательный атом, кислород стремится притянуть электроны атома водорода, поэтому на атомах водорода образуется частично положительный заряд. Т.е. возникает дипольный момент (хотя молекула воды в целом нейтральна) и две соседние молекулы воды могут притягиваться.
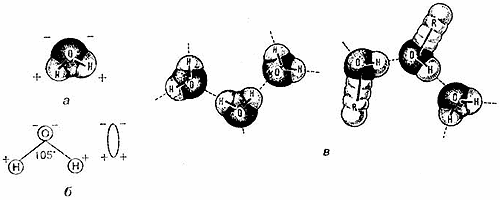
Рис.1. а - молекулярная модель молекулы воды ; б - диполь; в - гидратация за счет образования водородных связей между молекулами воды и другими соединениями (спирт).
Такой тип взаимодействий называется водородной связью. Она значительно слабее ковалентной. Такой тип связи характерен не только для воды, но и для многих органических соединений, например: