Учение о скорости химических реакции в организме и факторах, влияющих на нее, называется химической кинетикой. В химической кинетике скорость реакции определяется как изменение концентрации реагирующих веществ, происходящее в единицу времени.
Скорость реакции зависит от строения молекул реагирующих веществ, их концентрации, температуры, давления, наличия катализаторов и некоторых других факторов.
Реакция становится возможной только при столкновениях молекул. Чем больше молекул в единице объема, тем чаще они сталкиваются друг с другом, тем быстрее преобразуются. Однако, не каждое столкновение реагирующих молекул приводит к их изменению. Чтобы реакция началась, молекулы должны обладать определенным запасом энергии, необходимым
для преодоления энергетического барьера, который создается межмолекулярными силами отталкивания и внутримолекулярными силами сцепления (прочностью химических связей). Особенно много энергии нужно для разрыва ковалентных связей, преобладающих в молекулах органических веществ. Когда энергетический барьер преодолен и реакция началась, в ходе ее может выделиться значительно больше энергии, чем затрачено на начало процесса. Изменения энергии, происходящее в ходе химических реакций может быть изображено графически (Рис.1). Количество энергии, необходимое грамм-молекуле реагирующего вещества для вступления в реакцию, называется энергией активации и рассчитывается в кДж/моль.
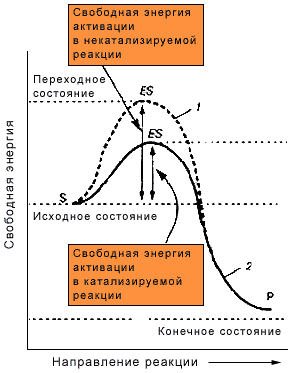
Рис.1 Изменение энергии в ходе химической реакции
Чем больше в веществе активных (возбужденных) молекул, способных преодолеть энергетический барьер, тем выше скорость его химических превращений. В обычных условиях только незначительная часть молекул вещества находится в активном состоянии. Активация их происходит при увеличении температуры, концентрации реагирующих веществ, увеличении давления (если это газообразные вещества).
В живых организмах большие колебания температуры и давления невозможны, поэтому большинство химических реакций в живых организмах идет с участием ферментов (или биологических катализаторов), которые снижают энергию активации реагирующих молекул во много раз за счет уменьшения сил отталкивания между молекулами и ослабления внутримолекулярных связей. Влияние ферментов настолько сильно, что имеющейся в организме тепловой энергии оказывается достаточно для активации реагентов.